Xét nghiệm Mycoplasma tự động trong 1 giờ, ứng dụng trong sản xuất sinh học
GIỚI THIỆU
Các dược điển khác nhau trong đó bao gồm USP, kiểm nghiệm thử nghiệm nhiễm khuẩn mycoplasma phải được thực hiện như một phần của kiểm tra thành phẩm được sản xuất với sự có mặt của tế bào nhân chuẩn.
Các phương pháp tuân thủ dược điển hiện tại đều yêu cầu ≥ 28 ngày để ra kết quả cuối cùng, tạo ra sự chậm trễ trong việc xuất xưởng thành phẩm. Các phương pháp xét nghiệm dựa trên acid nucleic thông thường (NAT). Tuy nhiên, cho đến gần đây các phương pháp này cung cấp tốc độ (~ 5 giờ) nhưng không dễ sử dụng.
Hệ thống Industry BIOFIRE® FILMARRAY® 2.0 sử dụng hệ thống FilmArray và thử nghiệm PCR thế hệ tiếp theo, trong đó tất cả các thành phần thuốc thử được chứa trong bộ kit để phát hiện >130 loài mycoplasma. Hệ thống cung cấp mẫu để phản hồi trong ~ 1 giờ mà không cần được đào tạo kỹ thuật.
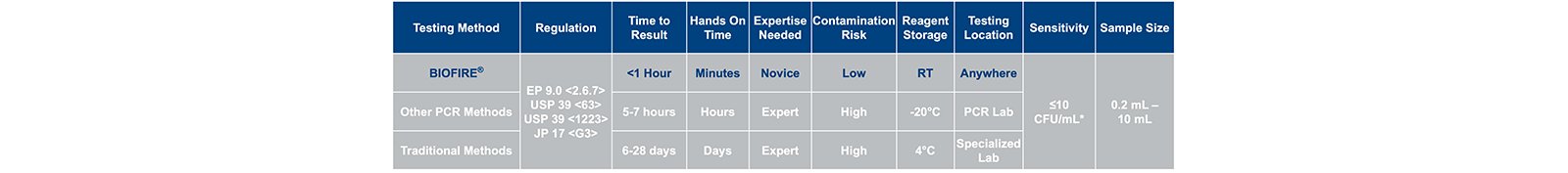
*10 mL protocol
Nội dung về kiểm nghiệm Mycoplasm được trình bày tại Hội nghị Vi sinh dược phẩm PDA năm 2021, dữ liệu được tóm tắt trong white paper từ bốn nhà sản xuất sản xuất sinh học đã đánh giá hệ thống Industrial BIOFIRE®FILMARRAY® 2.0. Các mẫu được kiểm tra với tối đa 9 loài mycoplasma tổng hợp, với sự có mặt của kháng thể đơn dòng mật độ cao được sản xuất từ tế bào buồng trứng chuột đồng Trung Quốc (CHO).
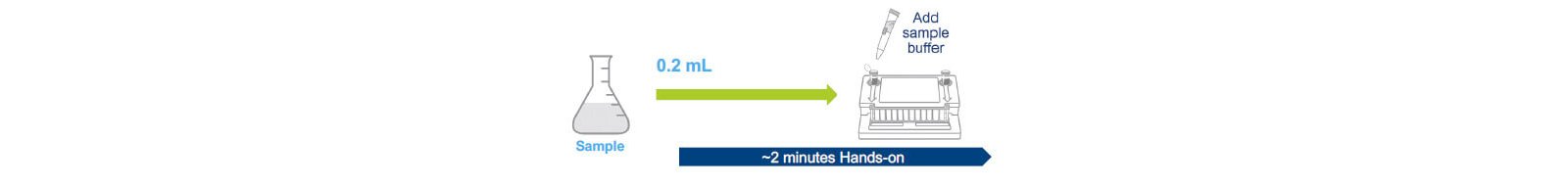
Các nghiên cứu được thiết kế để đánh giá tỷ lệ dương tính giả và tỷ lệ âm tính giả bao gồm mức độ phát hiện (LOD). Hai phương pháp riêng biệt đã được đánh giá: một phương pháp sử dụng 10 mL mẫu sản phẩm cung cấp độ nhạy để thử nghiệm xuất xưởng và phương pháp kiểm tra trực tiếp sử dụng mẫu sản phẩm 0,2 mL cho phép thử nghiệm kiểm soát trong quá trình online.
GIÁ TRỊ CỦA QUY TRÌNH KIỂM NGHIỆM MYCOPLASMA NHANH CHÓNG, DỄ DÀNG
Một phương pháp thử nghiệm nhanh hơn, dễ dàng hơn để kiểm nghiệm mycoplasma có thể mang lại giá trị cho các nhà sản xuất sản xuất. Trong đó bao gồm yêu cầu đào tạo đơn giản hơn, giảm thiểu các lỗi liên quan đến con người, đến việc cung cấp cảnh báo sớm về nhiễm khuẩn, kiểm nghiệm mycoplasma cực nhanh, cực kỳ dễ dàng, tiết kiệm thời gian và chi phí. Do đó sẽ mang lại giá trị cho bất kỳ đơn vị sản xuất nào. Kiểm nghiệm mycoplasma BIOFIRE® có thể được thực hiện bởi bất kỳ ai, bất cứ nơi nào vào bất cứ thời điểm nào, cho phép các nhà sản xuất thực hiện kiểm tra chất lượng quan trọng với những lợi ích sau:
• Đơn giản hoá quá trình đào tạo và không yêu cầu người vận hành có chuyên môn cao.
• Kết quả kiểm nghiệm Mycoplasma khách quan.
• Ít rủi ro lỗi thao tác của người vận hành/ Cải thiện tính toàn vẹn dữ liệu.
• Không yêu cầu thử nghiệm PCR.
• Thời gian trả kết quả 1 giờ mang lại sự linh hoạt trong việc lập kế hoạch kiểm tra.
• Cung cấp cảnh báo sớm về ô nhiễm và giảm chi phí phát sinh.

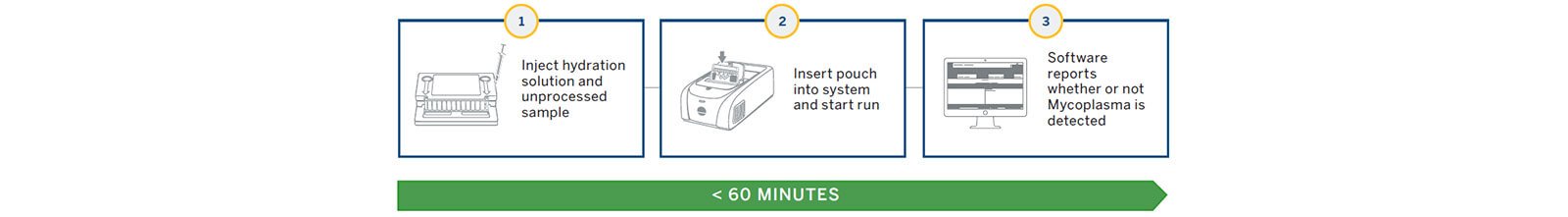
HỆ THỐNG INDUSTRY BIOFIRE FILMARRAY 2.0
Hệ thống sử dụng thiết bị Industry FILMARRAY® 2.0 và xét nghiệm PCR thế hệ tiếp theo bằng bộ kit để phát hiện ra mycoplasma (Hình 1 và 2). Bộ kít BIOFIRE® Mycoplasma dùng một lần chứa tất cả các thuốc thử cần thiết để ly giải tế bào tự động, tinh chế axit nucleic, phiên mã ngược, PCR I và PCR II kết quả là có thể phát hiện phân tích để phân lập, khuếch đại và phát hiện hơn 130 loài mycoplasma khác nhau (Hình 2).
Dụng cụ và phần mềm xử lý kết quả trong vòng chưa đầy một giờ.
Phần mềm Industry FILMARRAY® 2.0 (hoàn toàn đáp ứng yêu cầu 21 CFR Phần 11) thực hiện tất cả các phân tích tổng hợp phức tạp và cung cấp kết quả dưới dạng “Phát hiện ra Mycoplasma” hoặc “Không phát hiện Mycoplasma”.
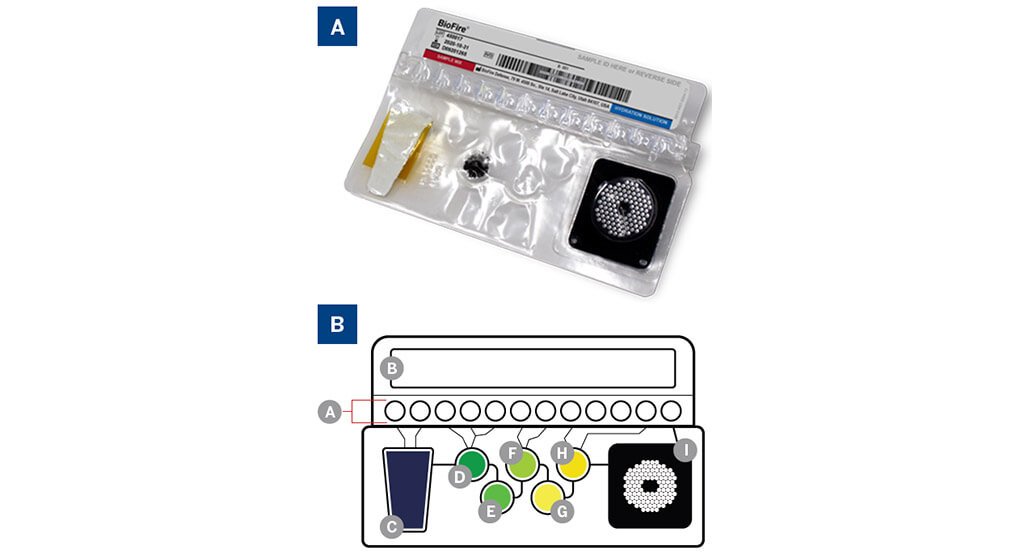
A. Túi Mycoplasma BIOFIRE®.
B. Sơ đồ bộ kit: (A) Thuốc thử đông khô; (B) Pít tông cung cấp thuốc thử cho bọt khí; (C) Ly giải mẫu và thu thập hạt; (D) Rửa; (E) Vỉ thu gom hạt từ tính; (F) Sự pha trộn; (G) Vỉ PCR bên ngoài ghép kênh; (H) Vỉ pha loãng; (I) Mảng PCR lồng nhau bên trong.
PROTOCOL
Hai protocol riêng biệt đã được thiết kế để kiểm tra mycoplasma (3). Thử nghiệm trực tiếp 0,2 mL có thể được sử dụng để kiểm tra đối chứng trong quá trình với LOD đã được xác nhận là ~ ≤30 CFU/mL và thử nghiệm giải phóng 10 mL tập trung mẫu bằng cách ly tâm và có LOD được xác nhận là ≤ 10 CFU/mL.
Các protocol này được tuân theo bởi các nhà đánh giá ngoại trừ Evaluator B sai khác với các khuyến nghị của nhà sản xuất với thời gian và lực ly tâm tùy chỉnh. Sau khi xử lý trước mẫu, các mẫu sau đó được nạp vào một bộ kit được chuẩn bị đầy đủ và hydrat hoá và chạy trên thiết bị Industry FILMARRAY® 2.0.